
مقدمة المنتج
| معلومات أساسية عن الفلوروسيتوسين |
| نظرة عامة آلية العمل والمقاومة الحركية الدوائية والجرعة السمية والآثار الجانبية المراجع |
| اسم المنتج: | الفلوروسيتوسين |
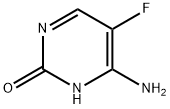
| المرادفات: | 4-أمينو-5-فلورو-2(1 ساعة) - بيريميدينون؛4-أمينو -5-فلورو -2(1H) - بيرميدينون؛ {{10} }فلوروسيتوسين؛5-فلوروسيتوسين؛5-فلوروسيتوسين؛فلوسيتوسين؛4-أمينو-5-فلورو-2(1H) - بيريميدين، فلوسيتوزين، {{19} }FC;5-فلوروسيتوسين98% |
| كاس: | 2022-85-7 |
| مف: | C4H4FN3O |
| ميغاواط: | 129.09 |
| اينكس: | 217-968-7 |
| فئات المنتجات: | النيوكليوتيدات والنيوكليوتيدات؛ مضادات الفطريات للاستخدام البحثي والتجريبي؛ الكيمياء الحيوية؛ الكواشف الكيميائية لأبحاث الصيدلة؛ القواعد النووية ونظائرها؛ النيوكليوسيدات والنيوكليوتيدات والكواشف ذات الصلة؛ سلسلة بيريميدين؛ حمض فينيل أسيتيك؛ الكيتون؛ الأحماض النووية؛ القواعد والكواشف ذات الصلة؛ النيوكليوتيدات؛ الأمينات ؛حلقات غير متجانسة؛بيريميدين؛بيريدين، بيريميدين، بورينات وبتيريدين؛API؛أمين |كيتون| ألكيل فلورين؛جلوكوترول؛مضاد للسرطان؛2022-85-7 |
| ملف مول: | 2022-85-7.مول |
 |
|
| الخواص الكيميائية للفلوروسيتوسين |
| نقطة الانصهار | 298-300 درجة (ديسمبر) (مضاءة) |
| كثافة | 1.3990 (تقديري) |
| ضغط البخار | 0باسكال عند 25 درجة |
| الدفع في الأفق. | 2-8 درجة |
| الذوبان | قابل للذوبان بشكل طفيف في الماء، وقابل للذوبان بشكل طفيف في الإيثانول (96 في المائة) |
| استمارة | مسحوق بلوري |
| pka | 3.26 (عند 25 درجة) |
| لون | الأبيض إلى الأبيض تقريبا |
| الذوبان في الماء | 1.5 جم/100 مل (25 درجة مئوية) |
| حساس | حساسة للضوء |
| ميرك | 14,4125 |
| بي آر إن | 127285 |
| فئة بي سي إس | 1 |
| استقرار: | حساسة للضوء |
| InChIKey | XRECTZIEBJDKEO-UHFFFAOYSA-N |
| سجلP | -1.36 عند 22.1 درجة وpH6.4-6.9 |
| التفكك ثابت | 2.74-10.71 عند 21.4 درجة |
| مرجع قاعدة بيانات CAS | 2022-85-7(مرجع قاعدة بيانات CAS) |
| معلومات السلامة |
| رموز المخاطر | إكسن، تي، شي |
| بيانات المخاطر | 40-36/37/38-63 |
| بيانات السلامة | 22-24/25-45-36/37-36/37/39-27-26 |
| دبليو جي كيه ألمانيا | 2 |
| RTECS | ها6040000 |
| F | 10-23 |
| ملاحظة المخاطر | سامة/حساسة للضوء |
| فئة المخاطر | مهيجة، حساسة للضوء |
| رمز النظام المنسق | 29335990 |
| بيانات المواد الخطرة | 2022-85-7(بيانات المواد الخطرة) |
| تسمم | LD50 in mice (mg/kg): >2000 شفويا و الشوري. 1190 إب; 500 الرابع (جرونبيرج، 1963) |
| معلومات MSDS |
| مزود | لغة |
|---|---|
| 2-هيدروكسي-4-أمينو-5-فلوروبيريميدين | إنجليزي |
| سيجما الدريخ | إنجليزي |
| أكروس | إنجليزي |
| ألفا | إنجليزي |
| استخدام الفلوروسيتوسين والتوليف |
| ملخص | تم تطوير البيريميدين المفلور، 5-فلوسيتوسين (فلوروسيتوسين؛ 5-FC، الشكل 1)، في البداية كعامل محتمل مضاد للسرطان ولكنه لم يكن فعالًا بدرجة كافية في مجال العلاج الكيميائي للسرطان.[1]. لاحقًا، أثبت 5-FC أنه نشط في داء المبيضات التجريبي وداء المكورات الخفية في الفئران[2]وكان يستخدم لعلاج الالتهابات البشرية[3]. بالإضافة إلى نشاطه ضد المبيضات والمكورات المستخفية، فإن 5-FC لديه أيضًا نشاط مثبط ضد الفطريات المسببة لداء الكروموبلاستوما[4]; ومع ذلك، فهو غير فعال ضد الالتهابات التي تسببها الفطريات الخيطية. 5-يتمتع FC بارتفاع معدل انتشار المقاومة الأولية في العديد من الأنواع الفطرية. بسبب هذه المقاومة الأولية، 5-يتم استخدام FC بشكل أساسي مع مضادات الفطريات الأخرى (في المقام الأول الأمفوتيريسين B، AmB) ومؤخرًا تم اختباره مع عوامل أخرى بما في ذلك الفلوكونازول (FLU)، والكيتوكونازول (KTZ)، إيتراكونازول (ITRA)، فوريكونازول (VORI)، وإشينوكاندين (على سبيل المثال، ميكافونجين، ميكا وكاسبوفونجين، كاس). يتم استخدامه فقط نادرا كعامل واحد. فلوسيتوزين (5-FC) هو مركب صناعي مضاد للفطريات، تم تصنيعه لأول مرة في عام 1957. ليس له قدرة جوهرية مضادة للفطريات، ولكن بعد أن يتم تناوله بواسطة الخلايا الفطرية الحساسة، يتم تحويله إلى 5- فلورويوراسيل ( 5-FU)، والذي يتم تحويله أيضًا إلى مستقلبات تمنع تخليق الحمض النووي الريبي (RNA) والحمض النووي (DNA) الفطري. العلاج الأحادي بـ 5-FC محدود بسبب التطور المتكرر للمقاومة. بالاشتراك مع الأمفوتريسين B، يمكن استخدام 5-FC لعلاج حالات الفطريات الجهازية الشديدة، مثل داء المستخفيات، وداء المبيضات، وداء الفطار الأرومي الصبغي، وداء الرشاشيات. 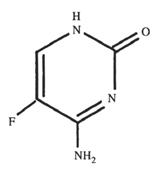 الشكل 1 التركيب الكيميائي للفلوروسيتوسين |
| آلية العمل والمقاومة | 5-FC هو الأكثر نشاطًا ضد الخمائر، بما في ذلك Candida وTorulopsis وCryptococcus spp.، وضد الفطريات الدموية المسببة لداء الكروموسومات (Phialophora وCladosporium spp.) وAspergillus spp.[5]تختلف MICs لـ {{0}}FC من 0.1 إلى 0.25 ملغم/لتر لهذه الأنواع الفطرية. في Emmonsia crescens، وEmmonsia parva، وMadurella mycetomatis، وMadurella grisea، وPyrenochaeta romeroi، وCephalosporium spp.، وSporothrix schenckii، وBlastomyces dermatitidis، تتراوح مستويات MICs من 100 إلى 1000 ملجم/لتر. 14 5-FC نشط أيضًا ضد بعض الأوليات، بما في ذلك Acanthamoeba culbertsoni سواء في المختبر أو في الجسم الحي و الليشمانيا النيابة. في المرضى.[5] ينتج النشاط المضاد للفطريات لـ 5-FC من تحوله السريع إلى 5-فلورويوراسيل (5-FU) بواسطة إنزيم نازعة أمين السيتوزين، داخل الخلايا الفطرية الحساسة. هناك آليتان يستخدم بهما 5-الفلورويوراسيل لممارسة نشاطه المضاد للفطريات. تتضمن الآلية الأولى تحويل 5- فلورويوراسيل من خلال 5- أحادي فوسفات الفلوروريدين (FUMP) و5- ثنائي فوسفات الفلوروريدين (FUDP) إلى 5- ثلاثي فوسفات الفلوروريدين (FUTP).[6]. يتم دمج FUTP أيضًا في الحمض النووي الريبي الفطري بدلاً من حمض اليوريليك؛ يؤدي هذا إلى تغيير التحلل الأميني للحمض النووي الريبوزي الناقل، ويزعج تجمع الأحماض الأمينية ويمنع تخليق البروتين[6]. الآلية الثانية هي استقلاب 5-FU إلى 5-فلوروديوكسيوريدين أحادي الفوسفات (FdUMP) بواسطة بيروفوسفوريلاز أحادي فوسفات اليوريدين.[6]. FdUMP هو مثبط قوي لسينثاز الثيميديلات، وهو إنزيم رئيسي يشارك في تخليق الحمض النووي والانقسام النووي.[7]. ومن ثم، يعمل 5-FC عن طريق التدخل في استقلاب البيريميدين وتخليق البروتين في الخلية الفطرية. يؤدي هذا النشاط إلى تحلل الخلايا والموت. لقد تم وصف حدوث المقاومة باستخدام 5-FC على نطاق واسع ويمنع استخدام 5-FC كعامل واحد[8, 10]يمكن التمييز بين آليتين أساسيتين للمقاومة: (1) يمكن أن تؤدي بعض الطفرات إلى نقص في الإنزيمات الضرورية للنقل الخلوي وامتصاص 5-FC أو استقلابه (أي نفاذية السيتوزين أو بيروفوسفوريلاز أحادي فوسفات اليوريدين أو نازعة أمين السيتوزين );[9,11](2) قد تنتج المقاومة من زيادة تخليق البيريميدينات، التي تتنافس مع مضادات المستقلبات المفلورة لـ 5-FC وبالتالي تقلل من نشاطها المضاد للفطريات.[9]لقد ثبت أن بيروفوسفوريلاز أحادي فوسفات اليوريدين المعيب هو النوع الأكثر حدوثًا لمقاومة FC 5-المكتسبة في الخلايا الفطرية.[12]أفاد Normark & Schönebeck أنه يمكن التعرف على نوعين ظاهريين مختلفين من السلالات المقاومة للـ FC 5-:[10]لا تتأثر سلالات النمط الظاهري للمقاومة من الفئة 1 بـ 5-FC بتركيزات عالية (هذه هي السلالات المقاومة تمامًا (جوهريًا))، بينما تكون سلالات الفئة 2 عرضة لـ 5-FC بتركيزات منخفضة ولكن، بعد التعرض لفترة طويلة لـ 5-FC (حتى عند التركيزات العالية) تتطور المقاومة (يقال إنها مقاومة جزئيًا أو اكتسبت مقاومة). من المحتمل أن يكون تطور المقاومة في السلالات الأخيرة ناتجًا عن اختيار طفرات غير حساسة، مما يؤدي إلى ظهور مجموعة مقاومة ثانوية.[9] يختلف معدل حدوث المقاومة لـ 5-FC بين الأنواع.20 تم العثور على ما يصل إلى 7-8% من السلالات المقاومة جوهريًا بين عزلات C. albicans، والمبيضات غير المحددة، وTorulopsis glabrata. في C. neoformans يكون معدل حدوث المقاومة أقل (1-2٪)، ولكن في Candida spp. بخلاف C. albicans تبلغ 22%، وذلك بسبب انتشار الأنواع الأقل حساسية بشكل عام مثل Candida Tropicalis وCandida krusei.[13]. إن معدل حدوث مقاومة 5-FC الأساسية ليس واضحًا. أفاد باحثون مختلفون أن معدلات الإصابة تتراوح بين 8% و44% بالنسبة لأنواع المبيضات Candida spp[14]. تشمل العوامل المحتملة التي تساهم في هذا النطاق الواسع طرق الحساسية المستخدمة، والعوامل المحلية التي تنطوي على استخدام العوامل المضادة للفطريات والاختلافات في انتشار أنواع المبيضات المختلفة.[14]. |
| الدوائية والجرعة | 5-يتم امتصاص FC بسرعة كبيرة وبشكل كامل تقريبًا: 76-89% يتوفر بيولوجيًا بعد تناوله عن طريق الفم.[16]في المرضى الذين يعانون من وظائف الكلى الطبيعية، يتم الوصول إلى التركيزات القصوى في المصل وسوائل الجسم الأخرى خلال 1-2 ساعة.[15, 16]. 5-يتغلغل FC بشكل جيد في معظم مواقع الجسم، بما في ذلك السوائل النخاعية والجسم الزجاجي والصفاقي، وفي المفاصل الملتهبة، لأنه صغير الحجم وقابل للذوبان في الماء بشكل كبير ولا يرتبط ببروتينات المصل إلى حد كبير[15-17]. 5-يتم التخلص من FC بشكل أساسي عن طريق الكلى وترتبط تصفية الدواء من البلازما ارتباطًا وثيقًا بتصفية الكرياتينين[15, 17]. 5-يتم استقلاب FC في الحد الأدنى فقط في الكبد. يتم التخلص الكلوي عن طريق الترشيح الكبيبي. ولا يحدث أي ارتشاف أو إفراز أنبوبي. عمر النصف لـ 5-FC هو c.3-4 ساعات في المرضى الذين يعانون من وظائف الكلى الطبيعية، ولكن يمكن تمديده حتى 85 ساعة في المرضى الذين يعانون من قصور كلوي حاد.[12, 16, 18]يغير القصور الكلوي 5-الحركية الدوائية لـ FC لأنه يبطئ الامتصاص ويطيل نصف عمر المصل ويقلل التصفية[15]. الحجم الظاهري لتوزيع 5-FC يقترب من إجمالي مياه الجسم ولا يتغير بسبب الفشل الكلوي. يجب تعديل الجرعة عند مرضى القصور الكلوي. وقد تم تقديم توصيات مختلفة[15-18]. اقترح Daneshmend & Warnock الإرشادات التالية لإدارة 5-FC للمرضى الذين يعانون من القصور الكلوي.[15]. In patients with a creatinine clearance of >40 مل / دقيقة، وينبغي استخدام جرعة قياسية قدرها 37.5 ملغم / كغم كل 6 ساعات. إذا كانت تصفية الكرياتينين بين 20 و 40 مل / دقيقة، فإن الجرعة الموصى بها هي 37.5 ملغم / كغم كل 12 ساعة. في المرضى الذين يعانون من تصفية الكرياتينين<20 mL/ minute, the dose of 5-FC should be 37.5 mg/kg once daily. Finally, if the creatinine clearance is <10 mL/min, frequent determinations of 5-FC concentration should be used as guidance for the frequency of dosing. |
| السمية والآثار الجانبية | 5-من المعروف أن لدى FC بعض الآثار الجانبية البسيطة نسبيًا، مثل الغثيان والقيء والإسهال، كما أن له أيضًا آثارًا جانبية أكثر خطورة، بما في ذلك تسمم الكبد وتثبيط نخاع العظم. الآثار الجانبية للجهاز الهضمي، وهي الآثار الجانبية الأكثر شيوعًا والأقل ضررًا المرتبطة بعلاج 5-FC، تشمل الغثيان والإسهال، وفي بعض الأحيان، القيء وآلام البطن المنتشرة. تحدث في حوالي 6% من المرضى الذين يعالجون بـ 5-FC[18]. وعلى الرغم من أن هذه الآثار الجانبية عادة لا تكون شديدة؛ تم الإبلاغ عن حالتين من التهاب القولون التقرحي وانثقاب الأمعاء[19]. يمكن أن يحدث التسمم الكبدي أثناء علاج 5-FC. في معظم الحالات، ينطوي ذلك على زيادة في تركيزات الترانساميناسات والفوسفاتيز القلوي في المصل[20]. نسبة حدوث التسمم الكبدي تتراوح بين 0 و 25%[20]. إن أشد حالات السمية المرتبطة بعلاج 5-FC هي اكتئاب النخاع العظمي. كانت هناك عدة تقارير عن نقص الكريات البيض الخطير أو المهدد للحياة، نقص الصفيحات و/أو قلة الكريات الشاملة[21-23]. آلية سمية 5-FC لا تزال غير مفهومة بشكل كامل. من المحتمل أن بعض الآثار الجانبية الناجمة عن 5-FC، على سبيل المثال تسمم الكبد وتثبيط نخاع العظم، تعتمد على الجرعة، على الرغم من أن ليس كل التقارير تدعم هذه النظرية. علاوة على ذلك، تم افتراض أن تحويل 5-FC إلى مستقلبات معينة، خاصة 5-FU، يمكن أن يكون أحد آليات تطور السمية المرتبطة بـ 5-FC. |
| مراجع |
هايدلبرغ سي، تشودوري إن كيه، دانيبيرج بي وآخرون. البيريميدينات المفلورة، فئة جديدة من المركبات المثبطة للورم. طبيعة 1957; 179(4561): 663-666 جرونبيرج إي، تيتسورث إي، بينيت إم. النشاط العلاجي الكيميائي لـ 5-الفلوروسيتوسين. وكلاء مضادات الميكروبات Chemother 1963؛ 161:566-568 شرابة د، مادوف MA. علاج تعفن الدم بالمبيضات والتهاب السحايا بالمستخفية باستخدام 5-الفلوروسيتوسين. عامل مضاد للفطريات جديد. جاما 1968؛ 206(4): 830-832 بنسون JM, ناهاتا MC. الاستخدام السريري للعوامل المضادة للفطريات الجهازية. كلين فارم 1988؛ 7(6): 424-438 شولر، إتش جي (1980). فلوسيتوزين. في العلاج الكيميائي المضاد للفطريات، (Speller، DCE، Ed.)، الصفحات من 35 إلى 106. وايلي، تشيتشيستر. Waldorf AR, Polak A. آليات عمل 5-الفلوروسيتوسين. وكلاء مضادات الميكروبات Chemother 1983؛ 23(1):79-85 دياسيو آر بي، بينيت جي، مايرز سي. طريقة عمل 5-الفلوروسيتوسين. بيوكيم فارماكول 1978؛ 27(5):703-707 بولاك، أ. وشولر، إتش جيه (1975). طريقة عمل 5-الفلوروسيتوسين وآليات المقاومة. العلاج الكيميائي 21، 113-30. بولاك، أ. (1977). 5-حالة الفلوروسيتوسين الحالية مع إشارات خاصة إلى طريقة العمل ومقاومة الأدوية. المساهمات في علم الأحياء الدقيقة والمناعة 4، 158-67. نورمارك، س. وشونبيك، ج. (1973). دراسات مختبرية لمقاومة الفلوروسيتوسين 5- في Candida albicans وTorulopsis glabrata. العوامل المضادة للميكروبات والعلاج الكيميائي 2، 114-21. فاسولي، م. وكيريدج، د. (1988). عزل وتوصيف الطفرات المقاومة للفلوروبيريميدين في نوعين من المبيضات. حوليات أكاديمية نيويورك للعلوم 544، 260-3. فرانسيس، ب. والش، تي جيه (1992). الدور المتطور للفلوسيتوزين في المرضى الذين يعانون من نقص المناعة: رؤى جديدة في السلامة والحركية الدوائية والعلاج المضاد للفطريات. الأمراض المعدية السريرية 15، 1003-18. ميدوف، جي. وكوباياشي، جي إس (1980). استراتيجيات في علاج الالتهابات الفطرية الجهازية. مجلة نيو إنغلاند الطبية 302، 145-55. أرمسترونج، د. وشميت، إتش جي (1990). المخدرات القديمة. في العلاج الكيميائي للأمراض الفطرية، (Ryley، JF، Ed.)، الصفحات من 439 إلى 454. سبرينغر-فيرلاغ، برلين. دانيشمند، تي كيه ووارنوك، دويتشه فيله (1983). الحرائك الدوائية السريرية للأدوية المضادة للفطريات الجهازية. حركية الدواء السريرية 8، 17-42. كاتلر، آر إي، بلير، إيه دي وكيلي، إم آر (1978). حركية الفلوسيتوسين في الأشخاص الذين يعانون من وظائف الكلى الطبيعية والضعيفة. علم الصيدلة السريرية والعلاجات 24، 333-42. بلوك، إي آر، بينيت، جي إي، ليفوتي، إل جي، كلاين، دبليو جيه، ماكجريجور، آر آر وهندرسون، إل. (1974). فلوسيتوزين وأمفوتيريسين ب: تأثيرات غسيل الكلى على تركيز البلازما وتصفيتها. دراسات في الرجل. حوليات الطب الباطني 80، 613-7. شونيبيك، جيه، بولاك، أ، فيرنيكس، إم، وشولر، إتش جيه (1973). دراسات حركية الدواء على العامل المضاد للفطريات عن طريق الفم 5-الفلوروسيتوسين لدى الأفراد الذين يعانون من وظائف الكلى الطبيعية أو الضعيفة. العلاج الكيميائي 18، 321-36. بنسون، JM وناهاتا، MC (1988). الاستخدام السريري للعوامل المضادة للفطريات الجهازية. الصيدلة السريرية 7، 424-38. بينيت، جي (1977). فلوسيتوزين. حوليات الطب الباطني 86، 319-21. كوفمان، CA & الإطار، PT (1977). سمية نخاع العظم المرتبطة 5-بالعلاج بالفلوروسيتوسين. العوامل المضادة للميكروبات والعلاج الكيميائي 11، 244-7. شليغل، آر جيه، بيرنييه، جنرال موتورز، بيلانتي، جا، مايبي، دا، أوزبورن، جي بي، ستيوارت، جي إل وآخرون. (1970). داء المبيضات الشديد المرتبط بخلل التنسج الغدة الصعترية ونقص IgA وتأثيرات الخلايا الليمفاوية في البلازما. طب الأطفال 45, 926–36. ماير، ر. وأكسلرود، جيه إل (1974). فقر الدم اللاتنسجي المميت الناتج عن الفلوسيتوسين. مجلة الجمعية الطبية الأمريكية 228، 1573. |
| وصف | 5-الفلوروسيتوسين (5-FC)، وهو نظير بيريميدين مفلور، هو دواء أولي مضاد للفطريات اصطناعي يتم تحويله بواسطة نازعة أمين السيتوزين إلى 5- فلورويوراسيل. 5-يتم استقلاب الفلورويوراسيل، وهو دواء سام للخلايا يستخدم على نطاق واسع، إلى ريبو وديوكسيريبونوكليوتيدات مفلورة، مما يؤدي إلى تثبيط تخليق الحمض النووي والبروتين، والذي له تأثيرات متعددة بما في ذلك تثبيطالمبيضاتالأنواع وج. المحدثونالالتهابات والسمية الخلوية تجاه الخلايا السرطانية. بالاشتراك مع ناقلات النسخ العكسي للفيروسات التي تحمل الجين المنشط لعقار السيتوزين دياميناز، تبين أن 5-FC يزيل بشكل انتقائي الخلايا السرطانية CT26 وTu-2449في المختبر(إيك50s=4.2 و1.5 ميكرومتر، على التوالي) ولتحسين البقاء على قيد الحياة بشكل ملحوظ وتقليل حجم الورم (بجرعة 500 مجم / كجم) في نموذجين مختلفين من الورم الدبقي الفأري المتزامن. |
| الخواص الكيميائية | الصلبة البلورية البيضاء |
| المنشئ | أنكوبون، روش، الولايات المتحدة، 1972 |
| الاستخدامات | 5-FC هو عامل سام مضاد للفطريات/مضاد للميكروبات |
| الاستخدامات | 5-يعمل الفلوروسيتوسين كعامل مضاد لمرض السكر ومضاد للفطريات ومضاد للميكروبات. وهو مفيد لعلاج الالتهابات الخطيرة التي تنشأ بسبب السلالات الحساسة من المبيضات أو Cryptococcus neoformans وداء الكروموسومات. علاوة على ذلك، يتم استخدامه في الدراسات المتعلقة بالتخليق الحيوي لـ TMP. |
| تعريف | ChEBI: فلوسيتوزين هو مركب فلور عضوي وهو السيتوزين الذي يتم استبداله في الموضع 5 بالفلور. دواء أولي لمضاد الفطريات 5-فلورويوراسيل، ويستخدم لعلاج الالتهابات الفطرية الجهازية. لها دور كدواء أولي. وهو مركب عضوي الفلورين، بيريميدون، أمينوبيريميدين، نظير النيوكليوسيد ودواء مضاد للفطريات بيريميدين. ويرتبط وظيفيا بالسيتوزين. |
| دواعي الإستعمال | فلوسيتوزين (أنكوبون) هو بيريميدين اصطناعي مفلور يرتبط هيكليا بالفلورويوراسيل (FU) والفلوكسوريدين. يمكن أن يكون فطريات وفطريات. على الرغم من أنه يستخدم بشكل متكرر في علاج الالتهابات الجهازية التي تسببها المبيضات والمكورات المستخفية، إلا أن المؤشرات الجلدية قد تشمل الالتهابات الناجمة عن داء الكروموسومات، وداء الشعريات المبوغة، وأنواع Cladosporium، وSporothrix. وهو غير فعال بشكل عام ضد أنواع الرشاشيات. |
| عملية التصنيع | يتم تقديم تحضير 5-فلورويوراسيل تحت عنوان "فلورويوراسيل". كما هو موضح في براءة الاختراع الأمريكية رقم 3,040,026، يتم بعد ذلك إخضاع 5-فلورويوراسيل للخطوات التالية لإعطاء فلوسيتوزين. الخطوة 1: 2،4-ثنائي كلورو-5-فلوروبيريميدين - خليط من 104 جرام (0.8 مول) من 5-فلورويوراسيل، و1,472 جرام (9.6 مول) من أوكسي كلوريد الفوسفور وتم تقليب 166 جرامًا (1.37 مول) من ثنائي ميثيل أنلين تحت الارتجاع لمدة ساعتين. بعد التبريد إلى درجة حرارة الغرفة، تمت إزالة أوكسي كلوريد الفوسفور بالتقطير عند 18 إلى 22 ملم و22 درجة إلى 37 درجة. تم بعد ذلك صب المادة المتبقية في خليط تم تقليبه بقوة مكون من 500 مل من الأثير و500 جرام من الثلج. بعد فصل طبقة الأثير، تم استخلاص الطبقة المائية بـ 500 مل، ثم 200 مل من الأثير. تم تجفيف أجزاء الأثير المجمعة فوق كبريتات الصوديوم، وترشيحها، وإزالة الأثير بواسطة التقطير الفراغي عند 10 درجة إلى 22 درجة. البقايا عبارة عن مادة صلبة صفراء منصهرة عند 37 درجة إلى 38 درجة، تزن 120 جرامًا أي ما يعادل 90٪ من العائد. التقطير الفراغي لـ 115 جرام من هذه المادة عند 74 درجة إلى 80 درجة (16 ملم) أعطى 108 جرام من ذوبان المادة الصلبة البيضاء عند 38 درجة إلى 39 درجة أي ما يعادل 84.5٪. الخطوة 2: 2-كلورو-4-أمينو-5-فلوروبيريميدين - إلى محلول 10.0 جرام ({{17}).{{27} }6 mol) من 2,4-ثنائي كلورو-5-فلوروبيريميدين في 100 مل من الإيثانول، تمت إضافة 25 مل من الأمونيا المائية المركزة ببطء. نتج عن ذلك حل براق قليلاً. وارتفعت درجة الحرارة تدريجياً إلى 35 درجة. تم بعد ذلك تبريد المحلول في الثلج إلى 18 درجة ثم بقي بعد ذلك أقل من 30 درجة. وبعد ثلاث ساعات، أظهرت معايرة فولهارد وجود 0.0545 مول من الكلور في الصورة الأيونية. أدى التخزين في الثلاجة طوال الليل إلى تبلور بعض كلوريد الأمونيوم. تم ملاط الحمأة البيضاء الناتجة عن تبخر خليط التفاعل عند 40 درجة مع 75 مل من الماء، وتم ترشيحها وغسلها خالية من الكلوريد. بعد التجفيف في الخلاء، ذاب المنتج عند 196.5 درجة إلى 197.5 درجة، وأنتج 6.44 جرام. أدى تبخر السائل الأم إلى إنتاج محصول ثان قدره 0.38 جرام، مما رفع إجمالي المحصول إلى 6.82 جرام (79.3%). الخطوة 3: 5-الفلوروسيتوزين - ملاط يحتوي على 34.0 جرام (0.231 مول) من 2-كلورو-4- أمينو-5- فلوروبيريميدين تم تسخين 231 مل من حمض الهيدروكلوريك المركز في حمام مائي عند درجة حرارة 93 درجة إلى 95 درجة لمدة 125 دقيقة. تمت متابعة التفاعل عن طريق القياس الطيفي للأشعة فوق البنفسجية باستخدام الامتصاص عند 245 و285 و300 mμ كدليل. ارتفع الامتصاص عند 300 ميكرومتر إلى الحد الأقصى بعد 120 دقيقة ثم انخفض قليلاً. تم تبريد المحلول الصافي إلى 25 درجة في حمام جليدي، ثم تم تبخيره حتى يجف تحت فراغ عند 40 درجة. بعد الملاط بالماء ثلاث مرات وإعادة التبخر، تمت إذابة المادة المتبقية في 100 ملليلتر من الماء. إلى هذا المحلول، المبرد بالثلج، تمت إضافة 29 مل من الأمونيا المركزة قطرة قطرة. يتم ترشيح الراسب الناتج، وغسله خاليًا من الكلوريد بالماء، ثم بالكحول والأثير. بعد التجفيف في وسط مفرغ عند 65 درجة، كان وزن المنتج 22.3 جرام. تم الحصول على 6.35 جرام إضافية عن طريق تبخر السائل الأم، وبالتالي الحصول على إجمالي 28.65 جرام (96.0%). |
| اسم العلامة التجارية | أنكوبون (فاليانت). |
| الوظيفة العلاجية | مضاد للفطريات |
| نشاط مضادات الميكروبات | يقتصر نطاق النشاط على Candida spp. وCryptococcus spp. وبعض الفطريات المسببة لمرض الكروموبلاستوما. |
| المقاومة المكتسبة | حوالي 2-3 من المبيضات النيابة. تكون العزلات (أكثر في بعض المراكز) مقاومة قبل بدء العلاج، وقد تتطور المقاومة أثناء العلاج. يبدو أن السبب الأكثر شيوعًا للمقاومة هو فقدان إنزيم بيروفوسفوريلاز يوريدين أحادي الفوسفات. |
| التطبيقات الصيدلانية | بيريميدين اصطناعي مفلور متاح للتسريب في الوريد أو تناوله عن طريق الفم. |
| إجراءات الكيمياء الحيوية/الفيزيولوجية | نظير النيوكليوزيد الذي له أنشطة مضادة للفطريات. 5-يتم تشتيت FC بواسطة نازعة أمين السيتوزين إلى المنتج 5-فلورويوراسيل، مما يؤدي إلى خطأ في تشفير الحمض النووي الريبي (RNA). 5-يمنع الفلوروسيتوسين تخليق DNA وRNA ويتداخل مع تخليق بروتين الريبوسوم. |
| آلية العمل | فلوسيتوزين (5-فلوسيتوسين، 5-FC؛ أنكوبان) هو نظير بيريميدين مفلور للسيتوزين الذي تم تصنيعه في الأصل للاستخدام المحتمل كعامل مضاد للأورام. يستخدم فقط لعلاج الالتهابات الجهازية الخطيرة التي تسببها السلالات الحساسة من Candida و Cryptococcus spp. تمت دراسة آلية عمل 5- الفلوروسيتوزين (5-FC) بالتفصيل. يدخل الدواء إلى الخلية الفطرية عن طريق النقل النشط على ATPases الذي ينقل البيريميدين عادة. بمجرد دخول الخلية، يتم تبليل الفلوروسيتوسين 5- في تفاعل يتم تحفيزه بواسطة نازعة أمين السيتوزين لينتج 5-فلورويوراسيل(5-FU). 5-الفلورويوراسيل هو المستقلب النشط للدواء.5-يدخل الفلورويوراسيل في مسارات تخليق كل من الريبونوكليوتيد والديوكسيريبونوكليوتيد. يتم دمج ثلاثي فوسفات الفلوروريبونوكليوتيد في الحمض النووي الريبي (RNA)، مما يسبب خللًا في تصنيع الحمض النووي الريبي (RNA). هذا المسار يسبب موت الخلايا. في سلسلة ديوكسيريبونوكليوتيد، يرتبط 5-فلوروديوكسيوريدين أحادي الفوسفات (F-dUMP) بـ 5،10-حمض ميثيلين رباعي هيدروفوليك، مما يقطع ركيزة تجمع الكربون الواحد التي تغذي تخليق الثيميديلات. وبالتالي، تم حظر تخليق الحمض النووي. |
| علم العقاقير | 5-يتم امتصاص FC بشكل جيد عن طريق الفم، بتوافر حيوي يزيد عن 90%. نصف عمر المصل هو 3 إلى 5 ساعات، مع مستويات المصل تصل إلى ذروتها بعد 4 إلى 6 ساعات بعد جرعة واحدة. يتم توزيع الدواء على نطاق واسع في سوائل الجسم، مع مستويات السائل النخاعي 60 إلى 80٪ من مستويات المصل. كما أن الدواء يخترق بشكل جيد في البول، والخلط المائي، وإفرازات الشعب الهوائية. يسمح الحد الأدنى من ارتباط بروتين المصل بإفراز أكثر من 90٪ من كل جرعة في البول؛ مطلوب تخفيض الجرعة بشكل كبير في وجود اختلال كلوي. 5-يمكن إزالة FC عن طريق غسيل الكلى وغسيل الكلى البريتوني. 5-قد يحدث تحويل FC إلى مستقلبات سامة في خلايا الثدييات إلى حد محدود، وهو ما يفسر 5-سمية FC. |
| الدوائية | الامتصاص عن طريق الفم: كامل Cالأعلى25 مجم / كجم 6- كل ساعة عن طريق الفم: 70-80 مجم / لتر بعد 1-2 ساعة نصف عمر البلازما: 3-6 ساعات حجم التوزيع: 0.7–1 لتر/كجم ربط بروتين البلازما ج. 12% يكون الامتصاص أبطأ عند الأشخاص الذين يعانون من اختلال وظائف الكلى، ولكن التركيزات القصوى تكون أعلى. تبلغ المستويات في السائل الدماغي الشوكي حوالي 75% من تركيز المصل المتزامن. يتم إخراج أكثر من 90% من جرعة الفلوسيتوسين في البول دون تغيير. يكون عمر النصف في المصل أطول بكثير في حالة الفشل الكلوي، مما يستلزم تعديل نظام الجرعة: بالنسبة للمرضى الذين لديهم تصفية الكرياتينين أقل من 40 مل / دقيقة، يجب مضاعفة الفاصل الزمني للجرعة إلى 12 ساعة؛ في حالة الفشل الكلوي الوخيم، ينبغي زيادة الفاصل الزمني بين الجرعات إلى مرة واحدة يوميًا أو أقل، بناءً على قياسات تركيز الدواء في المصل بشكل متكرر. |
| الاستخدام السريري | يمتلك فلوسيتوزين نشاطًا مضادًا للفطريات بشكل كبير ضد C. albicans، وأنواع المبيضات الأخرى، وC. neoformans، والكائنات الفطرية المسؤولة عن داء الكروموسومات. لا يعتبر الدواء المفضل لهذه الالتهابات الفطرية، 5-يظل FC مفيدًا كجزء من العلاج المركب لداء المبيضات الجهازي والتهاب السحايا بالمستخفيات وكدواء بديل لداء الكروموسومات. عندما يتم استخدامه كعلاج وحيد، فإن المقاومة والفشل السريري شائعان. تشمل الآليات المحتملة لمقاومة الأدوية انخفاض نفاذية غشاء الخلية الفطرية وانخفاض مستويات نازعة أمين السيتوزين الفطرية. العلاج المركب مع الأمفوتريسين ب والفلوسيتوزين في علاج التهاب السحايا بالمكورات العقدية وعدوى المبيضات العميقة الجذور، مثل التهاب المفاصل الإنتاني والتهاب السحايا، يسمح بتخفيض جرعات الأمفوتريسين ب ويمنع ظهور 5-مقاومة FC. عند استخدام جرعات أعلى من الأمفوتيريسين ب، فإن العلاج المركب مع 5-FC لا يمنح أي فائدة سريرية إضافية باستثناء علاج التهاب باطن المقلة بالمبيضات، حيث يظل اختراق الأنسجة مشكلة. |
| الاستخدام السريري | داء المبيضات (بالاشتراك مع الأمفوتريسين ب أو الفلوكونازول) داء المستخفيات (بالاشتراك مع الأمفوتريسين ب أو الفلوكونازول) من المستحسن مراقبة تركيزات الفلوسيتوسين في جميع المرضى، وهي إلزامية في المرضى الذين يعانون من اختلال كلوي. |
| آثار جانبية | الغثيان والقيء وآلام البطن والإسهال شائعة. وتشمل الآثار الجانبية الخطيرة كبت نقي العظم والسمية الكبدية. تحدث بشكل متكرر أكثر عندما تتجاوز تركيزات المصل 100 ملغم / لتر. يمكن أن تؤدي التأثيرات السمية الكلوية للأمفوتريسين ب إلى ارتفاع تركيزات فلوسيتوزين في الدم، ويجب مراقبة مستويات الدواء الأخير عند إعطاء هذه المركبات معًا. عندما يتم وصف 5-FC بمفرده للمرضى الذين يعانون من وظائف الكلى الطبيعية، يمكن أن يحدث طفح جلدي وضيق شرسوفي وإسهال وارتفاع في إنزيمات الكبد. |
| توليف | يتم تصنيع فلوسيتوزين، 5-فلوروسيتوسين (35.4.4)، من فلورويوراسيل (30.1.3.3). يتفاعل الفلورويوراسيل مع أوكسي كلوريد الفوسفور في ثنائي ميثيلانيلين لينتج 2,4-ثنائي كلورو-5-فلوروبيريميدين (35.4.2)، والذي يتفاعل مع الأمونيا لتكوين منتج مستبدل بالكلور في الموضع الرابع من حلقة البيريميدين —4-أمينو- 2-كلورو-5-فلوروبيريميدين (35.4.3). التحلل المائي لجزء الكلوروفينيل من هذا المركب في محلول حمض الهيدروكلوريك يعطي الفلوسيتوسين المطلوب.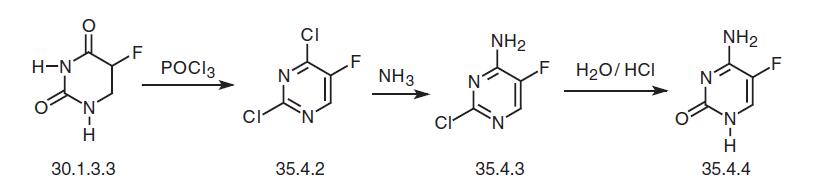 هناك طريقة بديلة للتخليق تتمثل في صنع فلوسيتوزين من مادة فلورويوراسيل — 5-فلورو-2- ميثيل ثيويوراسيل (30.1.3.2) باستخدام مخطط مشابه إلى حد ما. معالجة 5-فلورو-2- ميثيل ثيويوراسيل (30.1.3.2) مع خماسي كلوريد الفوسفور يعطي 4-كلورو-5-فلورو-2- ميثيل ثيوبيريميدين (35.4.5)، والذي عند تفاعله مع الأمونيوم يتحول إلى 4-أمينو-5-فلورو-2- ميثيلثيوبيريميدين (35.4.6). التحلل المائي لجزء الميثيلثيوفينيل باستخدام حمض الهيدروبروميك المركز يعطي الفلوسيتوسين المطلوب. 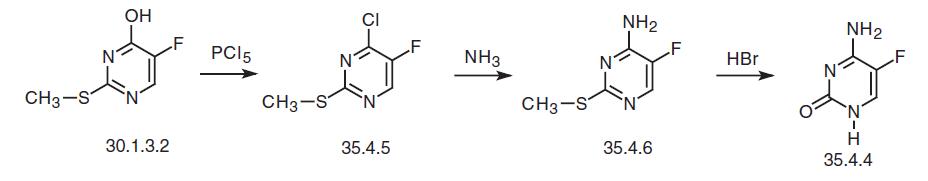 |
| تفاعل الأدوية | التفاعلات الخطرة المحتملة مع أدوية أخرى السيتارابين: من المحتمل أن ينخفض تركيز الفلوسيتوسين. |
| الاسْتِقْلاب | إن فلوسيتوزين في حد ذاته ليس سامًا للخلايا ولكنه دواء مساعد يتم تناوله عن طريق الفطريات ويتم استقلابه إلى 5- فلورويوراسيل (5-FU) بواسطة نازعة أمين السيتيدين الفطرية. بعد ذلك، يتم تحويل 5-FU إلى 5-فلوروديوكسيوريدين، والذي يتداخل، باعتباره مثبط سينسيز الثيميديلات، مع كل من التخليق الحيوي للبروتين والحمض النووي الريبوزي (RNA). 5-الفلورويوراسيل سام للخلايا ويستخدم في العلاج الكيميائي للسرطان. لا تحتوي الخلايا البشرية على نازعة أمين السيتوزين، وبالتالي، لا تحول الفلوسيتوسين إلى 5-FU. ومع ذلك، تقوم بعض النباتات المعوية بتحويل الدواء إلى 5-FU، وبالتالي فإن التسمم البشري ينتج عن هذا التمثيل الغذائي. |
| منتجات تحضير الفلوروسيتوسين والمواد الخام |
| مواد خام | Phosphorus oxychloride-->N-Methylaniline-->5-Fluorouracil-->4-Amino-2-chloro-5-fluoropyrimidine-->2,4-Dichloro-5-fluoropyrimidine-->5-FLUORO-4-HYDROXY-2-METHOXYPYRIMIDINE-->أوكسي كلوريد الفوسفور |
| منتجات التحضير | 2',3'-ثنائي-O-أسيتيل-5'-ديوكسي-5-فولورو-D-سيتيدين |
الوسم : الفلوروسيتوسين، الصين الفلوروسيتوسين المصنعين والموردين والمصنع
قد يعجبك ايضا
إرسال التحقيق







