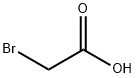
| الخواص الكيميائية |
كتلة بلورية بيضاء إلى صفراء فاتحة |
| الاستخدامات |
التخليق العضوي، فصل الحمضيات أثناء الحصاد. |
| الاستخدامات |
يستخدم حمض البرومو أسيتيك في التركيب العضوي وكعامل ألكلة. كما يستخدم كمادة كيميائية حيوية لأبحاث تحليل البروتينات. وهو مادة خام ووسيط مهم يستخدم في التركيب العضوي والمستحضرات الصيدلانية والأصباغ والمواد الكيميائية الزراعية. |
| الاستخدامات |
يستخدم حمض البرومو أسيتيك بشكل أساسي فيN- بروموآسيلة الطرفية للببتيدات المرتبطة بالراتنج.
يمكن استخدامه أيضًا:لتوليف (Z)-2-(سيكلوك-4-و-1-يلوكسي)حمض الأسيتيك.
لتحضير -برومو-فينيل أسيتاميد.
لتحويل ثيوسيميكاربازونات العطرية إلى ثيازوليل هيدرازونات.
|
| الوصف العام |
محلول مائي. |
| تفاعلات الهواء والماء |
قابل للذوبان في الماء. |
| ملف التفاعلية |
تتبرع الأحماض الكربوكسيلية، مثل حمض البرومو أسيتيك، بأيونات الهيدروجين إذا كانت هناك قاعدة موجودة لتقبلها. تتفاعل بهذه الطريقة مع جميع القواعد، سواء العضوية (على سبيل المثال، الأمينات) أو غير العضوية. تصاحب تفاعلاتها مع القواعد، والتي تسمى "التحييدات"، تطور كميات كبيرة من الحرارة. ينتج التحييد بين حمض وقاعدة ماء بالإضافة إلى ملح. تذوب الأحماض الكربوكسيلية التي تحتوي على ست ذرات كربون أو أقل بحرية أو بشكل معتدل في الماء؛ تذوب الأحماض التي تحتوي على أكثر من ست ذرات كربون قليلاً في الماء. تتفكك الأحماض الكربوكسيلية القابلة للذوبان إلى حد ما في الماء لإنتاج أيونات الهيدروجين. وبالتالي فإن الرقم الهيدروجيني لمحاليل الأحماض الكربوكسيلية أقل من 7.0. تتفاعل العديد من الأحماض الكربوكسيلية غير القابلة للذوبان بسرعة مع المحاليل المائية التي تحتوي على قاعدة كيميائية وتذوب حيث ينتج التحييد ملحًا قابلاً للذوبان. يمكن للأحماض الكربوكسيلية في المحاليل المائية والأحماض الكربوكسيلية السائلة أو المنصهرة أن تتفاعل مع المعادن النشطة لتكوين الهيدروجين الغازي وملح معدني. تحدث مثل هذه التفاعلات من حيث المبدأ للأحماض الكربوكسيلية الصلبة أيضًا، ولكنها بطيئة إذا ظل الحمض الصلب جافًا. حتى الأحماض الكربوكسيلية "غير القابلة للذوبان" قد تمتص ما يكفي من الماء من الهواء وتذوب بدرجة كافية في حمض البرومو أسيتيك لتآكل أو إذابة أجزاء وحاويات الحديد والصلب والألومنيوم. تتفاعل الأحماض الكربوكسيلية، مثل الأحماض الأخرى، مع أملاح السيانيد لتوليد سيانيد الهيدروجين الغازي. يكون التفاعل أبطأ للأحماض الكربوكسيلية الجافة الصلبة. تتفاعل الأحماض الكربوكسيلية غير القابلة للذوبان مع محاليل السيانيد لتسبب إطلاق سيانيد الهيدروجين الغازي. تتولد الغازات القابلة للاشتعال و/أو السامة والحرارة من تفاعل الأحماض الكربوكسيلية مع مركبات الديازو، ومركبات ثنائي ثيوكربامات، وإيزوسيانات، ومركبتان، ونيتريدات، وكبريتيدات. تتفاعل الأحماض الكربوكسيلية، وخاصة في المحاليل المائية، مع الكبريتيت والنتريت والثيوكبريتات (لإنتاج كبريتيد الهيدروجين وكبريتات الكبريتات) والديثيونيتات (SO2)، لتوليد غازات قابلة للاشتعال و/أو سامة والحرارة. ويؤدي تفاعلها مع الكربونات والبيكربونات إلى توليد غاز غير ضار (ثاني أكسيد الكربون) ولكن مع ذلك الحرارة. ومثل المركبات العضوية الأخرى، يمكن أكسدة الأحماض الكربوكسيلية بواسطة عوامل مؤكسدة قوية واختزالها بواسطة عوامل اختزال قوية. وتولد هذه التفاعلات الحرارة. ومن الممكن إنتاج مجموعة متنوعة من المنتجات. ومثل الأحماض الأخرى، قد تبدأ الأحماض الكربوكسيلية تفاعلات البلمرة؛ ومثل الأحماض الأخرى، فإنها غالبًا ما تحفز (تزيد من معدل) التفاعلات الكيميائية. |
| خطر |
مهيج قوي للجلد والأنسجة. |
| خطر على الصحة |
سامة؛ قد يؤدي استنشاق أو ابتلاع أو ملامسة (الجلد والعينين) للأبخرة أو الغبار أو المواد إلى إصابة خطيرة أو حروق أو وفاة. قد يؤدي ملامسة المادة المنصهرة إلى حروق شديدة في الجلد والعينين. سيؤدي التفاعل مع الماء أو الهواء الرطب إلى إطلاق غازات سامة أو أكالة أو قابلة للاشتعال. قد يولد التفاعل مع الماء قدرًا كبيرًا من الحرارة مما يزيد من تركيز الأبخرة في الهواء. ستنتج النار غازات مزعجة أو أكالة و/أو سامة. قد يكون الجريان السطحي من مياه مكافحة الحرائق أو التخفيف تآكليًا و/أو سامًا ويسبب التلوث. |
| خطر الحريق |
مادة قابلة للاشتعال: قد تحترق ولكنها لا تشتعل بسهولة. تتفاعل المادة مع الماء (بعضها بعنف) فتطلق غازات قابلة للاشتعال أو سامة أو تآكلية ومياه جارية. عند تسخينها، قد تشكل الأبخرة مخاليط متفجرة مع الهواء: في الأماكن المغلقة والمفتوحة ومخاطر انفجار المجاري. معظم الأبخرة أثقل من الهواء. تنتشر على طول الأرض وتتجمع في المناطق المنخفضة أو المحصورة (المجاري والأقبية والخزانات). قد تنتقل الأبخرة إلى مصدر الاشتعال وتعود. قد يتطور غاز الهيدروجين القابل للاشتعال عند ملامسته للمعادن. قد تنفجر الحاويات عند تسخينها أو إذا تلوثت بالماء. |
| قابلية الاشتعال والانفجار |
غير قابل للاشتعال |
| ملف السلامة |
السم عن طريق الابتلاع، عن طريق الصفاق، وعن طريق الوريد. مهيج ومسبب للتآكل للجلد والأغشية المخاطية. تم الإبلاغ عن بيانات الطفرة. عند تسخينه حتى التحلل، ينبعث منه أبخرة سامة من البروميد. انظر أيضًا البروميدات. |
| طرق التنقية |
يتم بلورة حمض البرومو أسيتيك من إيثر بيتا كلورايد (ب 40-60o). يتم تمرير محلول إيثر ثنائي الإيثيل منه عبر عمود أكسيد الألومنيوم، ويتم تبخير الإيثر في درجة حرارة الغرفة تحت الفراغ. يتم الحصول عليه بشكل أفضل عن طريق التقطير من Claisen (قارورة مغمورة في حمام زيت) مزودة بعمود فيجرو معزول (ص 11) ويتم جمع الكسر ب 108-110o/30 مم. وهو حساس للضوء والرطوبة. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] مُدمع ومُهيج للجلد. |